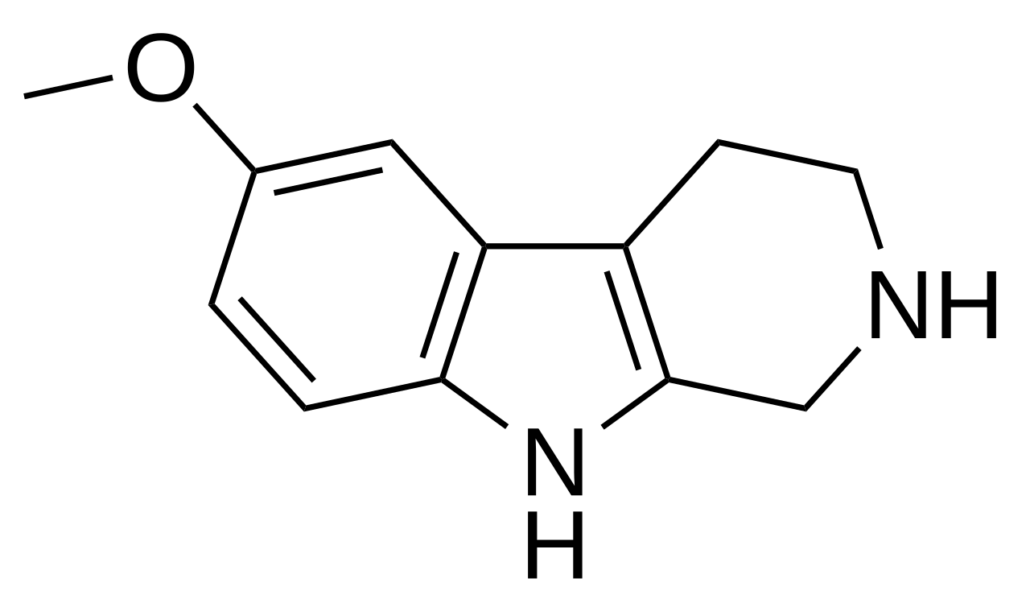
La pinolina tra mito e scienza
La pinolina (6-MeO-THBC) è una β-carbolina, o meglio una tetraidro-β-carbolina, la cui presenza endogena è molto controversa.
Presenza nel corpo umano
Studi degli anni 70′ e 90′ avevano rilevato la pinolina nella ghiandola pineale utilizzando tecniche poco selettive [1].
Tuttavia lavori più moderni che hanno impiegato metodi più avanzati, come la cromatografia liquida associata a spettrometria di massa tandem (LC/MS/MS), non hanno trovato la betacarbolina in questa ghiandola [2].
La sua origine precisa ad oggi non è chiara, ma si ipotizza che venga prodotta nel sistema nervoso centrale , non specificatamente dalla ghiandola pineale.
Un derivato della melatonina?
Un delle ipotesi più plausibili è che la pinolina si formi localmente nel tessuto nervoso tramite la reazione di Pictet-Spengler, una sintesi chimica fondamentale che converte una triptamina (come la serotonina) e un composto carbonilico (aldeide in questo caso) in una betacarbolina [3].
Anche la melatonina è una triptamina e quindi un potenziale candidato per questa reazione, ma le sue caratteristiche strutturali e la sua minore reattività la rendono meno plausibile in questo scenario rispetto alla serotonina.
Un altro ormone del sonno?
L’ipotesi di un coinvolgimento della pinolina nella regolazione del sonno nasce dall’analogia con altre indolamine come la melatonina. Tuttavia, l’assenza di evidenze riproducibili sulla sua presenza in vivo, unita alla mancanza di un meccanismo biosintetico e di bersagli molecolari definiti, rende questa ipotesi difficilmente sostenibile alla luce delle conoscenze attuali.
La sua rilevanza fisiologica nell’organismo umano rimane incerta.
Farmacologia
Analogamente ad altre tetraidro-β-carboline, la pinolina è un inibitore dell’enzima monoamina ossidasi A (MAO-A) estremamente debole, farmacologicamente poco significativo (IC50 = 41.5 ± 6.3 µM).
E’ molto potente invece come stimolatore della neurogenesi in vitro, un’azione probabilmente mediata dalle sue proprietà serotoninergiche: come gli psichedelici ha mostrato un’azione multirecettoriale che comprende 5-HT1A, 5-HT2A, 5-HT2B, 5-HT2C, 5-HT7 e il trasportatore SERT [4].
La pinolina è dotata inoltre di una marcata attività antiossidante.
Nel modello animale di epatossicità da tetracloruro di carbonio ha protetto il fegato delle cavie dai danni ossidativi e dalla rigidità della membrana [5].
In altri studi ha ridotto la perossidazione lipidica indotta dalla tossicidà da alluminio [6] e da lipopolisaccaridi [7], suggerendo un potenziale effetto protettivo nei confronti dei danni ossidativi.
Nel 2006 Bausch & Lomb, un’azienda americana produttrice di lenti, lenti a contatto ed altri prodotti riguardanti la vista e gli occhi, ha registrato una patente per un farmaco a base di questa molecola destinato al trattamento di diversi disordini oftalmici [8].
FONTI
8)Bartels, S. P. (2006) U.S. Patent No. 20,060,292,202 Washington, DC: U.S.
Tutte le informazioni presenti su questo sito sono fornite a solo scopo informativo ed educativo.
Non costituiscono in alcun modo invito all’uso improprio, a pratiche pericolose o a comportamenti contrari alla legge.
I contenuti relativi a etnobotanica, chimica e farmacologia delle specie trattate hanno finalità esclusivamente divulgative e non intendono suggerire usi medicinali o alimentari.
Eventuali descrizioni di effetti o sintomi da intossicazione sono riportate unicamente in un’ottica di informazione scientifica e riduzione del rischio.
I prodotti venduti (incensi, aromi naturali per ambienti, coloranti naturali, sementi, materiale botanico da esposizione) non sono destinati al consumo umano.
Si invita a leggere attentamente Termini e Condizioni prima di effettuare un eventuale acquisto.









One thought on “La pinolina tra mito e scienza”